MOKOは長年にわたり、お客様および適用される規制要件を常に満たす医療機器および関連サービスを提供してきました。厳格なISO13485の要件に基づき継続的に審査を受け、認証取得にふさわしい企業であることを繰り返し証明してきました。
ISO13485認証とは
ISO13485は、医療機器の適格性を審査するための究極のQMS(品質マネジメントシステム)規格です。その主な目的は、医療製品および関連サービスが最適な機能を発揮できるよう、最高品質であることを保証することです。医療資産の設計、開発、製造、サービス提供、保管、流通、設置を行う企業や組織は、消費者にサービスを提供する前に、これらの規制基準を満たす必要があります。MOKOは常にお客様の利益を最優先に考え、これらの基準を満たしています。
この認証は世界中で認められています。米国がISO 13485:13485を米国FDA 2016 CFR 21と整合させる取り決めを提案したことを受け、ISO820は現在、FDAの必須品質管理システムとなっています。ISO13485認証は、規制要件を満たしていれば、登録組織であれば規模を問わず取得できます。ただし、これは個人向けの規格ではないため、個人に発行することはできません。
ISO13485は製品規格ではないため、医療製品の品質を規定するものではありません。対象となる組織が遵守すべき製品ベースの規格です。
ISO13485認証プロセス
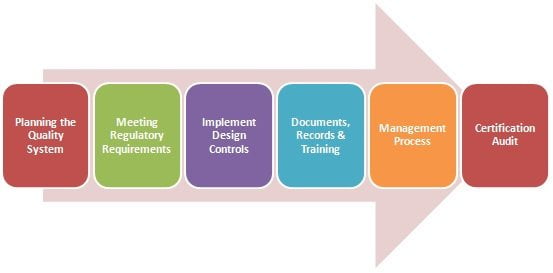
医療機器を扱うすべての組織は、厳格な要件を満たす必要があります。これは、医療機器の製造と提供に必要なプロセスを完全に理解していることを確認するためです。MOKOも例外ではありませんでした。ISO 13485認証を取得する前に、CB(認証機関)による徹底的な監査を受けました。認証の有効期間はXNUMX年間です。XNUMX年後には、再認証のために再度監査を受ける予定です。
これらの要件は定期的に更新されるため、一定期間後に再認証が必要になります。
認証プロセスは6段階に分かれています。まず、組織はQMSの変更を実施するために、品質マネジメントシステムを文書化し、提示する必要があります。次に、製品を販売する地域の規制要件を満たす必要があります。最後に、顧客のニーズに合わせて設計プロトコルを実装する必要があります。第13485段階では、組織は品質管理プロセスの記録とトレーニングに関する文書を提示する必要があります。第XNUMX段階では、認証委員会が組織のリスク管理プロセスを評価し、認証監査の最終段階に進みます。これは、医療分野の専門担当者とISOエージェントによって行われます。監査が完了すると、いくつかの是正計画が提案される場合があります。組織は、最終的なISOXNUMX認証を取得するために、これらの計画を受け入れる必要があります。
ISO13485認証がお客様にとって何を意味するか
医療機器が消費者の生死を左右する可能性があることは周知の事実です。このことを念頭に置き、MOKOは設計、開発、製造プロセスにおける品質管理監査の合格に常に努め、最終製品が消費者の生活を向上させることを保証しています。だからこそ、私たちはISO13485認証を何度も取得しているのです。
それ以外にも、当社はお客様のために全体的な業務を改善するために、UL、RoHS、ISO 14001、ISO 9001 の認証を取得しています。



